计算题:若HCL的密度为1.183g/ml,含HCL量为37%,计算此盐酸的物质的量的浓度?(已知HCL的摩尔质量是36.45g/mol)
第1题:
将10 mL浓HCl用50mL水稀释后的溶液应表示为( )。
A、1+5 HCl溶液
B、1→5 HCl溶液
C、1:5 HCl溶液
D、V1/V2=1/5的HCl溶液
第2题:
欲配制7%的HCl溶液500mL,需取36%的浓HCl多少毫升(7%、36%HCl密度分别为1.05g/cm3、1.18g/cm3)?
第3题:
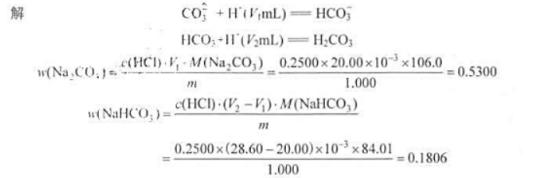
第4题:
用0.1mol·L-1NaOH溶液分别与HCl和HAc溶液各20ml反应时,均消耗掉20ml的NaOH,这表示()。
第5题:
计算题:若要配制0.5mol的HCL溶液1000ml。需2mol的HCL溶液多少?
第6题:
质量分数为36.0%的浓盐酸(密度1.19),其物质的量浓度C(HCL)为()。(注:HCL分子量为36.5)
A.42.84mol/L
B.36.0mol/L
C.12.06mol/L
D.11.74mol/L
第7题:
计算题:中和池内现在含HCL0.1%R的酸性废液2000m3,欲将其中和达标排放,问需加入含NaOH30%工业烧碱多少m3(已知30%NaOH的密度为1.3g/cm3)。
第8题:
A、11.9
B、5.8
C、23.8
D、36.5
第9题:
含CaCl2和HCl的水溶液,移取20.00ml,用0.1000mol/L的NaOH溶液滴定至终点,用去15.60ml,另移取 10.00ml试液稀释至50.00ml,通过强碱性阴离子交换树脂,流出液用0.1000mol/L的HCl滴至终点,用去22.50ml。则试液中HCl的浓度为()mol/L,CaCl2的浓度为()mol/L。
第10题:
实验室配制C(HCL)的盐酸溶液,要量取9mL的浓HCl,需()量取。