0.1000mol·L-1K2Cr2O7溶液对Fe3O4的滴定度(MFe3O4=231.55)为()
第1题:
用盐酸滴定液(0.1000mol/L)滴定20ml NH3·H20溶液(0.1000mol/L),化学计量点的pH值为( )。
A.9.94
B.9.70
C.8.72
D.7.O0
E.5.27
第2题:
此题为判断题(对,错)。
第3题:
用氢氧化钠滴定液(0.1000mol/L)滴定20ml醋酸溶液(0.1000mol/L),化学计量点的pH值为
A.8.72
B.7.O0
C.5.27
D.4.30
E.3.50
第4题:
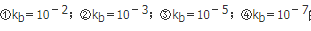
第5题:
用氢氧化钠滴定液(0.1000mol/L)滴定20.00ml盐酸溶液(0.1000mol/L),滴定突跃范围的pH是( )
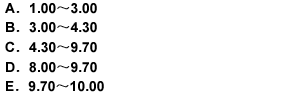
第6题:
用氢氧化钠滴定液(0.1000mol/L)滴定20ml醋酸溶液(0.1000mol/L),化学计量点的pH为
A.8.72
B.7.00
C.5.27
D.4.3
E.3.5
第7题:
用C(NaOH)0.1000mol/L的NaOH溶液滴定C(H2SO4)0.1000mol/LH2SO4溶液20.00ml,以甲基红为指示剂,问终点时需要消耗NaOH溶液多少毫升?
第8题:
用盐酸滴定液(0.1000mol/L)滴定20mlNH4C1溶液(0.1000mol/L),化学计量点的pH值为
A.9.94
B.9.70
C.8.72
D.7.00
E.5.27
第9题:
用NaOH滴定液(0.1000mol/L)滴定20.00ml盐酸溶液(0.1000mol/L)时,其滴定突跃的pH范围为( )
A.7.74~9.70
B.5.3~8.7
C.4.3~9.7
D.3.3~10.7
E.6.24~4.30
第10题: