极慢反应过程的传递速率远比反应速率快得多,液相中溶解的A接近其饱和溶解度,化学反应在液膜中进行,反应速率代表了A的传递速率。
第1题:
A、接近0
B、接近其饱和浓度
C、先升高,后降低
D、维持某一高浓度不变
第2题:
A.接近饱和浓度
B.接近0
C.先升高,后降低
D.不断升高直至接近饱和浓度
第3题:
A、气膜传质过程
B、液膜传质过程
C、气、液膜传质过程
D、化学反应过程
第4题:
受单体的浓度变化影响最大的是()。
第5题:
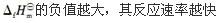

第6题:
反应的活化能是什么?它是怎样影响化学反应速率的?为什么有些反应的活化能很接近,反应速率却相差很大、但有些反应的活化能相差较大,反应速率却很接近?
答案:反应的活化能是指化学反应中,由反应物分子到达活化分子所需的最小能量。
化学反应速率与其活化能的大小密切相关。活化能越低,反应速率越快,因此降低活化能会有效地促进反应的进行。
从碰撞理论给出的公式k=Ae-Ea/RT 可以看出,Ea以指数关系影响速率常数k值,它的确是影响反应速率的重要因素,但A也影响k值。对不同的反应,A对k的影响很大,所以活化能不是决定反应速率的唯一因素。
第7题:
在选择化工过程是否采用连续操作时,下述几个理由不正确的是( )。
A.操作稳定安全
B.一般年产量大于4500t的产品
C.反应速率极慢的化学反应过程
D.工艺成熟
第8题:
A、填料塔
B、喷洒塔
C、鼓泡塔
D、搅拌釜
第9题:
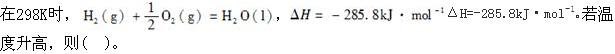
第10题:
在选择化工过程是否采用连续操作时,下述几个理由不正确的是()。