高中化学《物质的分类》
一、考题回顾
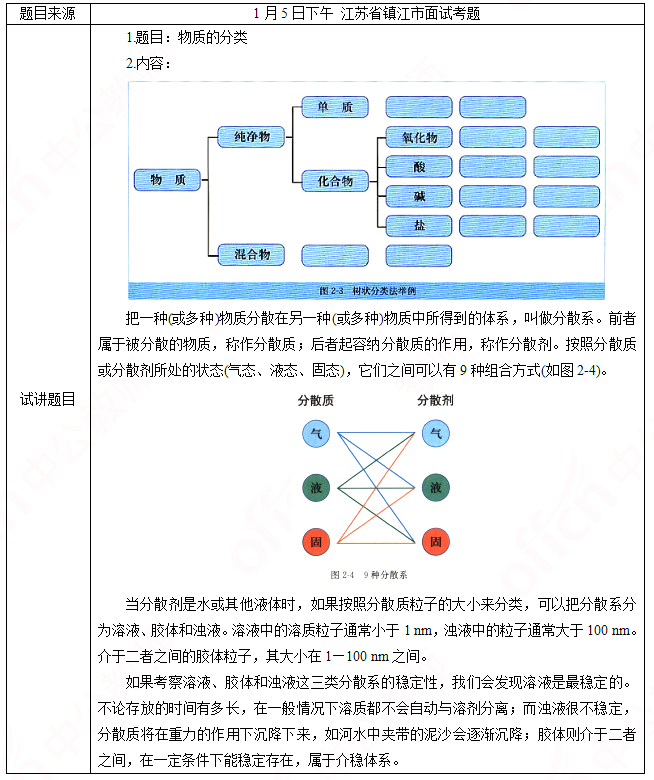

二、考题解析
【教学过程】
(一)导入新课
【教师提问】初中已经学习过物质的分类,那么按照物质组成成分的种类,可以把物质怎样进行分类呢?
【学生回答】分为纯净物和混合物。
【教师提问】可否进一步分类?
【学生回答】纯净物可以分为单质和化合物。
【教师引导】之前主要学习了纯净物的进一步划分,今天来研究混合物的进一步分类。
(二)新课教学
【教师提问】混合物通常是由一种物质或几种物质分散到另一种物质或几种物质中形成的。我们把这样的体系叫做分散系。阅读教材找到分散系的概念。
【学生回答】把由一种物质或几种物质分散到另一种物质或几种物质中形成的体系叫做分散系。
【提出问题】结合分散系、分散质、分散剂的概念,说一说对于硫酸铜溶液、泥水来说什么是分散质、分散剂?
【学生回答】在分散系中,被分散的物质为分散质,分散其他物质的物质叫做分散剂。溶液中溶质分散质为硫酸铜固体,分散剂为水;浊液中分散质为泥,分散剂为水。
【提出问题】按照分散剂和分散质所处的状态(气态、液态、固态),它们有几种组合方式,并举出具体的实例。
【学生回答】气气(空气);液气(云雾);固气(灰尘);气液(泡沫);液液(酒);固液(泥水);气固(海绵);液固(珍珠);固固(合金)。括号外为分散质、括号内为分散剂。
【提出问题】按照分散质粒子的大小,能对分散系进行分类吗?
【学生回答】按分散质粒子的大小将分散系分为溶液、胶体和浊液。
【提出问题】将Fe(OH)3和泥水分别进行过滤,观察并记录你看到了什么现象,由此说明了什么?
【学生回答】胶体的分散质能通过滤纸孔隙,而浊液的分散质则不能,这说明浊液分散质粒子比胶体的大。
【提出问题】那么溶液和胶体的分散质粒子大小关系如何呢?想一想,腌制咸鸭蛋时,Na+、Cl-能透过蛋壳内壁的半透膜进入蛋白质内,而身为胶体粒子的蛋白质分子却不能透过半透膜,那么胶体粒子大小、溶液中粒子大小、半透膜孔径大小关系如何?
【学生回答】胶体粒子要比半透膜的孔径要大,溶液中粒子大小比半透膜的孔径要小。说明胶体分散质粒子大小>溶液中粒子大小。
【提出问题】结合刚才所做的实验和教材“科学史话”的内容,思考胶体的丁达尔效应与胶体粒子大小有什么关系,胶体能够发光吗?
【学生回答】可见光的波长在400~700 nm之间,胶体粒子的直径在1~100 nm之间,小于可见光的波长,能使光波发生散射;当光束通过胶体时,看到的光柱是被胶体粒子散射的现象,并不是胶体粒子本身发光。
【提出问题】思考为什么光通过溶液和浊液时,没有光亮的“通路”出现?
【学生回答】溶液也能发生光的散射,但由于溶液中粒子的直径小于1 nm,散射及其微弱。所以,当光束通过胶体时可观察到丁达尔效应,而通过溶液时则观察不到这种现象。
(三)拓展提高
【提出问题】胶体区别于其他分散质的本质特征是什么?
解析:是分散质粒子直径的大小,胶体能产生丁达尔效应就是与这一特征有关。
(四)小结作业
请学生回答本堂课的收获有哪些,可以回答学到了哪些知识,也可以回答学习的感受。
布置作业:胶体还有哪些性质,课下预习。
【板书设计】
.

【答辩题目解析】
1.如何制备氢氧化铁胶体?
2.谈谈实验在教学中的作用。


