某元素的最外层只有一个l=0的电子,则该元素不可能是哪个区的元素?()
第1题:
第2题:
某元素的原子核外有三层电子层,最外层电子数是核外电子数的1/6,该元素的元素符号是Mg。
第3题:
A、12
B、20
C、19
D、30
第4题:
某短周期元素的最外层电子数比次外层电子数少3个,该元素气态氢化物中的化合价为()
第5题:
某元素的非金属性强,一般是指()。
第6题:

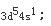

第7题:
某元素最外电子层上有两个电子,其量子数n=5,ι=0,它是哪个区的元素?()
第8题:
第9题:
某元素的金属性强,一般是指()。
第10题:
若某基态原子的外围电子排布为4d15s2,则下列说法正确的是()