已知0.1mol/L某一元弱酸的PH值为3,该弱酸溶液的电离度是:()
第1题:
某弱酸MOH的Kb=1答案:×10-5,则其0.1mol/L溶液的PH值为:( )
A.3.0
B.5.0
C.9.0
D.11.0
E.12.0
第2题:
浓度为0.1mol/L的某弱酸弱碱盐NH4A溶液pH=7.00,则HA的pKa为( )。
(已知:NH3·H2O的Kb=1.8×10-5)
求计算过程
答案:
NH4A在质子论当作两性物质 [H+]=约=[Ka(NH4+) *Ka(HA)]^1/2 [H+]^2 =Ka(NH4+)* Ka(HA) 而Ka(NH4+)=Kw/Kb(NH3) 因此 [H+]^2 =Kw/ Kb(NH3)* Ka(HA) (10^-7)^2=10^-14 /Kb(NH3)* Ka(HA) 即:Ka(HA)=Kb(NH3)=1.8*10^-5。
第3题:
此题为判断题(对,错)。
第4题:
缓冲溶液的PH值决定于构成该缓冲溶液的弱酸或弱碱的电离度。
第5题:
有一弱酸HR,在0.1mol·L-1的溶液中有2%电离,试确定该酸在0.05mol·L-1溶液中的电离度()
第6题:
此题为判断题(对,错)。
第7题:

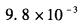
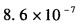
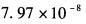
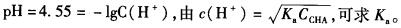
第8题:
某弱酸HAc的Ka=1(×)10-5,则其0.1mol/L溶液的PH值为:()?
A.1.0
B.2.0
C.3.0
D.3.5
E.5.0
答案:C
解析:因为是弱酸,所以HAc电离能力很弱,HAc浓度近似等于0.1mol/L,由Ka=【H+】*【Ac-】/【HAc】,【H+】和【Ac-】近似相等,可得【H+】=10-3,PH=-lg(氢离子浓度)所以PH值=3
第9题:
强碱滴定弱酸,理论终点时的溶液pH值与弱酸电离常数的关系是()。
第10题:
某一元弱酸,浓度为0.1mol·L-1,该溶液的pH=5.15,该一元弱酸的Ka值是()。