写出容量法测N2H4的化学反应方程式。取工业联氨0.1毫升(密度=1.0),消耗0.1摩尔/升Na2S2O3标准溶液3.45毫升,空白试验消耗Na2S2O335.62毫升,求工业联氨的浓度?(原子量:N=14)
第1题:
(2) 写出生成A的化学反应方程式_________________________________________。

第2题:
停炉保护中,满水保护法常采用 ________ 、N2H4法、氨液法,干法保护常采用 ________ 、充N2法、干燥剂法。
第3题:
(2)写出其中的一个化学方程式是48 ;
该化学反应的基本类型是49。
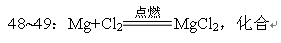
Mg +2HCl====MgCl2+H2↑,置换
Mg +CuCl2====MgCl2+Cu,置换
MgO+2HCl====MgCl2+H2O,复分解
Mg(OH)2+2HCl====MgCl2+2H2O,复分解
MgCO3+2HCl====MgCl2+H2O+CO2↑,复分解
MgSO4+BaCl2====MgCl2+BaSO4↓,复分解(说明:任写其中一个即可)
第4题:
氨合成反应的化学反应方程式:()
第5题:
工业联氨的浓度为40%(密度1.0),取0.1毫升工业联氨,用容量法测其浓度,至少应加0.05摩尔/升I2标准溶液多少毫升?
第6题:
(4) 写出C生成D的化学反应方程式:
__________________________________________________________________。
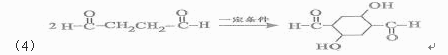
第7题:
写出水煤气发生炉制取水煤气的主要化学反应方程式?
第8题:
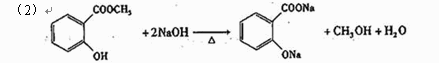
(2)写出A生成B和E的化学反应方程式_________ 。
第9题:
测给水N2H4应用()法,测停炉保护水N2H4应用()法。
第10题:
请写出铜火法精炼的氧化主要化学反应方程式。