取水样50mL,在25℃时,用0.0500mol∕L的HCl标准溶液滴定测定其碱度,首先用酚酞作指示剂,滴定至终点时,消耗HCl标准溶液1.2mL;之后,再向该水样中加甲基橙指示剂,用HC标准溶液继续滴定至终点,又消耗HCl标准溶液3.4mL。32则该水样中的酚酞碱度值为(),总碱度值为();该水样中的碱度成分为(),其含量分别为()。
第1题:
配制酸碱标准溶液时,用吸量管量取HCl,用台秤称取NaOH。
此题为判断题(对,错)。
第2题:
计算题:称取2.0131gNa2CO3试样,在容量瓶中配成250mL试液,用移液管吸取此液25mL,用c(HCl)=0.2019mol/L的HCl标准溶液滴定至终点,用去18.31mL,求该样中Na2CO3的质量分数。
解:反应式为
=0.9733=97.33(%)
答:该样中的Na2CO3质量分数为97.33%。
略
第3题:
A.取5mL至50mL容量瓶,加入条件试剂后定容
B.取10mL至50mL容量瓶,加入条件试剂后定容
C.取50mL蒸发浓缩到少于 50mL,转至50mL容量瓶,加入条件试剂后定容
D.取100mL蒸发浓缩到少于 50mL,转至50mL容量瓶,加入条件试剂后定容
第4题:
取20mL盐酸溶液,用0.0100mol/L的碳酸钠标准溶液标定时,恰好用了10mL碳酸钠标准溶液,则该盐酸溶液的浓度为()。
第5题:
称取2.0131gNa2CO3试样,在容量瓶中配成250mL试液,用移液管吸取此液25mL,用c(HCl)=0.2019mol/的HCl标准溶液滴定至终点,用去18.31ml,求该样中Na2CO3的质量分数?
反应式为Na2CO3+2HCl=2NaCl+CO2+H2O
Na2CO3的质量分数为
w(Na2CO3)=(c(HCl)v(HCl)M(1/2Na2CO3)/ms
=(0.2019³18.31³10-3³53.00)/2.0131³(25.00/250.00)
=0.9733=97.33%
该样中Na2CO3的质量分数为97.33%
略
第6题:
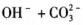
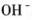
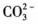
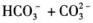

第7题:
在25℃时取水样50ml,用0.0500mol/L的标准盐酸溶液滴定碱度。首先,用酚酞作指示剂,滴定到终点消耗1.2ml,之后再向该水样中滴加甲基橙指示剂,至终点时又消耗3.4ml,计算出该水样中的碱度成分,并计算它们含量?
令P为酚酞碱度,M为甲基橙碱度。则
P=(0.05³1.2³103)/50=1.2mmol/L
M-P=(0.05³3.4³103)/50=3.4mmol/L
因为M-P>P,所以水样中仅有CO32-和HCO3-两种碱度成分。
c(1/2CO32-)=2P=2³1.2=2.4mmol/L
c(HCO3-)=(M-P)-P=3.4-1.2=2.2mmol/L
水样中仅有CO32-和HCO3-两种碱度成分,浓度分别是2.4mmol/L和2.2mmol/L。
略
第8题:
A、配制NaOH标准溶液用量筒取水
B、使用移液管之前,可将其烘干直接移取
C、标定HCl时,用酸式滴定管
D、标定HCl时,用NaOH固体
E、配制NaOH标准溶液时,准确称取后用蒸馏水溶解再定量转移至容量瓶中保存
第9题:
取50mL水样,调节pH=10.0,用0.025mol/L的EDTA标准洛液测定水样的硬度,消耗5.6mL,测水的硬度为()mg/L(CaC03)
第10题:
配制酸碱标准溶液时,为什么用量筒量取HCl,用台秤称取NaOH,而不用吸量管和分析天平?