一容器内贮有理想气体,压强为1.33Pa,温度为7℃,在平衡状态下,则单位体积(1m3)中的分子数为()。
第1题:
第2题:

第3题:
气体在容器内的状态会随着环境温度的变化而变化,如温度低于或等于临界温度时,容器内气体状态为气液两相共存状态。如温度高于临界温度时,容器内气体为气相状态。()
第4题:
气体在容器内的状态会随着环境温度的变化而变化,如温度低于或等于临界温度时,容器内气体状态为气液两相共存状态。如温度高于临界温度时,容器内气体为气相状态。
A对
B错
第5题:

第6题:

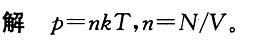
第7题:

第8题:
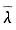 仅决定于( )。
仅决定于( )。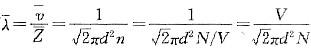 ,按题意,一定量的理想气体在容器中,其总分子数N不会改变,所以仅取决于体积V,故选(B)
,按题意,一定量的理想气体在容器中,其总分子数N不会改变,所以仅取决于体积V,故选(B)第9题:
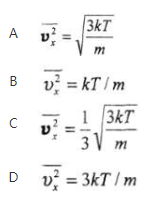
第10题:
理想气体状态方程是描述理想气体状态变化规律的方程。质量为m,摩尔质M的理想气体,其状态参量压强p、体积V和绝对温度t之间的函数关系为()