一个反应的活化能越高,反应速率越快。
第1题:
A、△rGmθ越负,反应速率越快。
B、△rHmθ越负,反应速率越快。
C、活化能越大,反应速率越快。
D、活化能越小,反应速率越快。
第2题:
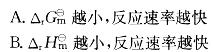
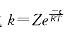 可知:温度一定时,活化能越小,速率常数就越大,反应速率也越大。
可知:温度一定时,活化能越小,速率常数就越大,反应速率也越大。第3题:
A.氧化还原反应速率越快
B.氧化还原反应速率越慢
C.氧化还原反应机理复杂
D.氧化还原反应的完全程度越高
第4题:
对于一个化学反应,下列说法中正确的是()
第5题:
活化能越大反应速度越快。
第6题:
反应的活化能是什么?它是怎样影响化学反应速率的?为什么有些反应的活化能很接近,反应速率却相差很大、但有些反应的活化能相差较大,反应速率却很接近?
答案:反应的活化能是指化学反应中,由反应物分子到达活化分子所需的最小能量。
化学反应速率与其活化能的大小密切相关。活化能越低,反应速率越快,因此降低活化能会有效地促进反应的进行。
从碰撞理论给出的公式k=Ae-Ea/RT 可以看出,Ea以指数关系影响速率常数k值,它的确是影响反应速率的重要因素,但A也影响k值。对不同的反应,A对k的影响很大,所以活化能不是决定反应速率的唯一因素。
第7题:
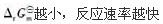
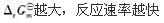

第8题:
A.放热越多,反应速率越快。
B.活化能越小,反应速率越快。
C.平衡常数越大,反应速率越快。
D.△rGmθ越大,反应速率越快。
第9题:
有关反应速率的叙述中错误的是()。
第10题:
活化能越大,反应速率越快,反应越容易进行。