欲使相同温度的两种稀溶液间不发生渗透,应使两溶液(A,B中的基本单元均以溶质的分子式表示)()。
第1题:
等渗溶液应是()
A、同一温度下,溶液的质量浓度相等的两溶液
B、物质的量浓度相等的两溶液
C、溶质的物质的量相等的两溶液
D、同一温度下的两种溶液
E、同一温度下,渗透浓度相等的两种溶液
第2题:
同体积、摩尔浓度相同的几种可溶性盐的溶液中,一定含有相同的( )。
A.溶质的质量
B.酸根离子数
C.溶质的物质量
D.金属离子数
第3题:
A.CaCI2
B.NaCI
C.NH3
D.C6H12O6
第4题:
第5题:


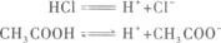
第6题:
此题为判断题(对,错)。
第7题:
物质的量浓度相同的两种酸,它们的质量百分浓度不一定相同。
此题为判断题(对,错)。
第8题:
9%NaCl溶液与血浆相同的是
A、胶体渗透压
B、K+浓度
C、Na+浓度
D、总渗透压
E、Ca2+浓度
第9题:

第10题:
同体积、同物质的量浓度的几种可溶性盐的溶液中,一定含有相同的()。
A溶质的物质的量
B溶质的质量
C酸根离子数
D金属离子数