①>②
①<②
①=②
不能确定
第1题:
等渗溶液应是()
A、同一温度下,溶液的质量浓度相等的两溶液
B、物质的量浓度相等的两溶液
C、溶质的物质的量相等的两溶液
D、同一温度下的两种溶液
E、同一温度下,渗透浓度相等的两种溶液
第2题:
如配制摩尔质量为Mb(g/mol),物质的量为nB(mol),体积V(L)的固体溶液,则其物质的量浓度为()。
第3题:
在一定条件下,对于密闭容器中进行的反应CO+NO2CO2+NO,下列说法中可以充分说明这一反应达到化学平衡状态的是( )。
A.CO、NO2 、CO2、NO四种物质的浓度相等
B.反应一段时间后,这四种物质的含量不随时间发生变化
C.CO、NO2 、CO2、NO四种物质在密闭容器中共存
D.正逆反应的速率相等且都为零
第4题:
取三个干燥的烧瓶,分别装入标准状况下的干燥氨气、含有二分之一体积空气的氯化氢、二氧化氮和氧气(体积比为4∶1)的混合气体;然后分别做溶解于水的喷泉实验。实验结束后三个烧瓶中所得溶液的物质的量浓度之比为()
第5题:


第6题:
A、蓝
B、红
C、紫
D、无
第7题:


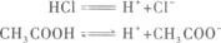
第8题:
滴定分析中,标准溶液的浓度表示方法为()
A、物质的量浓度
B、质量百分浓度
C、当量浓度
D、体积百分浓度
第9题:
第10题:
有关实验的叙述,正确的是()。