标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)各增加1V
标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)各减少1V
标准电动势Eθ不变,锌标准电极电势φθ(Zn2+/Zn)增加1V
标准电动势Eθ不变,锌标准电极电势φθ(Zn2+/Zn)减少1V
标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)均不变
第1题:
反应:Zn+2H+(xmol·dm-3)=Zn2+(1mol·dm-3)+H2(100kpa)构成的原电池的电动势为0.46V,φθ(Zn2+/Zn)=- 0.76V,则pH值为。
A、10.2
B、2.5
C、3
D、5.1
第2题:
把氧化还原反应Zn+2Ag+Zn2++2Ag组成原电池,欲使该原电池的电动势增大,可采取的措施是()
第3题:
此题为判断题(对,错)。
第4题:
在下列金属电对中,标准电极电势值最小的是()
第5题:
将氢电极(p(H2)=100kPa)插入纯水中,与标准氢电极组成一个原电池,则EMF=()
第6题:
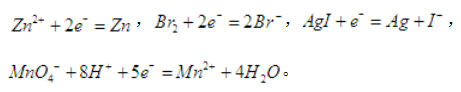
第7题:
有关标准氢电极的叙述,不正确的是()
第8题:
电对H+/H2,其电极电势随溶液的pH上升而;电对O2/OH-,其电极电势随溶液的pH上升而。
A、增加,增加
B、降低,降低
C、增加,降低
D、降低,增加
第9题:
(2012)在铜锌原电池中,将铜电极的c(H+)由1mol/L增加到2mol/L,则铜电极的电极电势:()
第10题:
对于电对Zn2+/Zn,增大其Zn2+的浓度,则其标准电极电势值将()