VB族
ⅢB族
VA族
ⅢA族
第1题:
第2题:

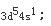

第3题:
第4题:
某短周期元素的最外层电子数比次外层电子数少3个,该元素气态氢化物中的化合价为()
第5题:
在元素周期表中,价层电子构型为ns2np3的元素有(),(),(),(),(),称为()元素;价层电子构型为(n1)d10ns2np6的元素有(),(),(),这类元索属于()。
第6题:
第7题:
某元素最高正价与负价绝对值之差为4,该元素的离子与跟其核外电子排列相同的离子形成的化合物是()
第8题:
A.1
B.3
C.2
D.4
第9题:
已知某元素+2价离子的核外电子排布式为:[Ar]3d5,该元素在周期表中处于()周期、()族、()区,元素符号是()。
第10题:
已知某副族元素A的原子,电子最后排入3d,最高氧化数为+4;元素B的原子,电子最后排入4p,最高氧化数为+5。回答下列问题: ⑴写出A、B元素原子的核外电子排布式。 ⑵根据核外电子排布式,指出它们在周期表中的位置(周期、族)。