第1题:
元素的化合价就是这种元素的原子与其他元素的原子形成化合物时得失或转移的电子数。( )
此题为判断题(对,错)。
第2题:
一些中性分子由于失去一个或几个电子,原子核的正电荷超过了电子的总电荷,称为正离子或()。
阳离子
略
第3题:
在燃烧或爆炸的氧化还原反应中的电子转移过程中,电子的接受体,在反应中被还原的物质,我们称为()。
A、还原剂
B、氧化剂
C、粘合剂
第4题:
已知A元素原子的L层比B元素原子的L层少3个电子,B元素原子的核外电子总数比A多5个,则A与B可形成()。
第5题:
康普顿效应是指()
第6题:
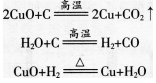

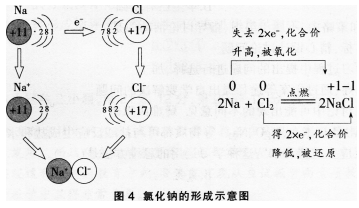
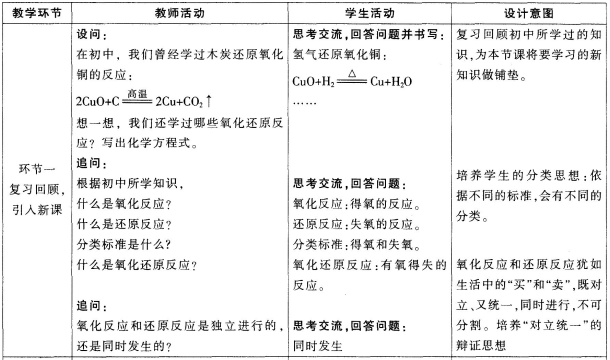



第7题:
过渡元素原子的电子能级往往是(n-1)d〉ns,但氧化后首先失去电子的是ns轨道上的,这是因为()
第8题:
A金属原子的价层电子数加上配位体所提供的配位电子总数之和等于8时,化合物较稳定
B金属原子的价层电子数加上配位体所提供的配位电子总数之和等于18时,化合物较稳定
C金属原子电子数加上配位体所提供的电子数之和等于18时,化合物较稳定
D金属原子电子数加上配位体所提供的电子数之和等于8时,化合物较稳定
第9题:
离子化合物中,原子失去电子形成()价,得到电子形成()价。
第10题:
氧化还原反应的实质就是物质间电子的得失或物质中原子间共用电子对的偏移。