葡萄糖
NaCl
CaCl2
蔗糖
第1题:
等渗溶液应是()
A、同一温度下,溶液的质量浓度相等的两溶液
B、物质的量浓度相等的两溶液
C、溶质的物质的量相等的两溶液
D、同一温度下的两种溶液
E、同一温度下,渗透浓度相等的两种溶液
第2题:
难溶电解质AgCl(s)在中溶解度最小。
A、0.1mol·L-1的NaCl溶液
B、0.1mol·L-1AgNO3溶液
C、纯水
D、0.2mol·L-1的NaCl溶液
第3题:
A、0.1mol/LMgSO4溶液和0.1mol/LCaCl2溶液
B、0.2mol/L蔗糖溶液和0.1mol/L果糖溶液
C、2mol/LNaCl溶液和4mol/L葡萄糖溶液
D、50g/L葡萄糖溶液和50g/L蔗糖溶液
E、以上都属于
第4题:
等渗溶液应是()。
第5题:
第6题:
将临床上使用的等渗溶液,如50g·L-1葡萄糖溶液和9g·L-1NaCl溶液按任意体积混合所得混合液仍为等渗溶液。()
第7题:
下列混合溶液具有缓冲作用的是。
A、0.2mol·L-1的NH4Cl和0.2mol·L-1的NaOH溶液等体积混合
B、0.2mol·L-1的NH4Cl和0.1mol·L-1的NaOH溶液等体积混合
C、0.2mol·L-1的HAc和0.2mol·L-1的NaOH溶液等体积混合
D、0.2mol·L-1的NaAc和0.2mol·L-1的HCl溶液等体积混合
第8题:
此题为判断题(对,错)。
第9题:
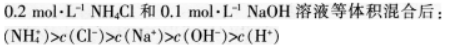
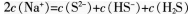
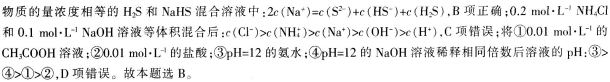
第10题:
物质的量浓度均为0.1mol•L-1的下列溶液,其渗透压最大的是()。