易形成—1价离子
从上到下原子半径逐渐减小
从上到下单质的氧化性逐渐减弱
从上到下氢化物的稳定性依次减弱
第1题:
A.第3周期ⅠA族元素
B.第2周期ⅡA族元素
C.第2周期ⅥA族元素
D.第3周期ⅦA族元素
第2题:
 族_______;
族_______;
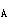 族_______。
族_______。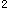 4s
4s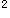 Te:5s
Te:5s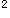 5p
5p
第3题:
关于元素周期表与周期律,下列说法正确的是
A、元素的性质随着原子量的递增,呈周期性变化
B、在元素周期表中,族序数都等于该元素的原子的最外层电子数
C、在元素周期表中,非金属性最强的元素,其最高价氧化物对应水化物的酸性也最强
D、随着核电荷数的递增,元素原子半径依次增大
E、ⅦA族单质自上而下,随原子量的增大,溶沸点升高
第4题:
在所有的金属中,熔点最高的是副族元素,熔点最低的也是副族元素
第5题:
IA族元素,最外层为1个电子,容易失去,性质活泼。
第6题:
第7题:
稀土金属属于()元素
第8题:
A、钾族和铀族
B、铀族和钍族
C、钾族和钍族
D、钾族、铀族和钍族
第9题:
比较铜族元素和锌族元素的通性.怎样说明锌族元素较同周期的铜族元素活泼
第10题:
Li是ⅠA族元素,但性质却与ⅡA族的金属Mg很相似,为什么?