高中化学《元素周期表》
一、考题回顾
题目来源1月6日上午 吉林省白城市面试考题
试讲题目1.题目:元素周期表
2.内容:
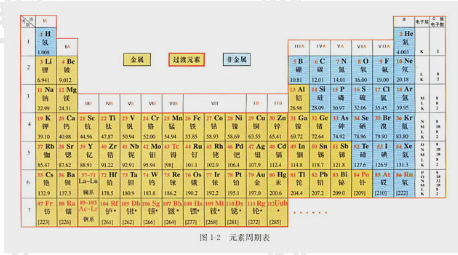
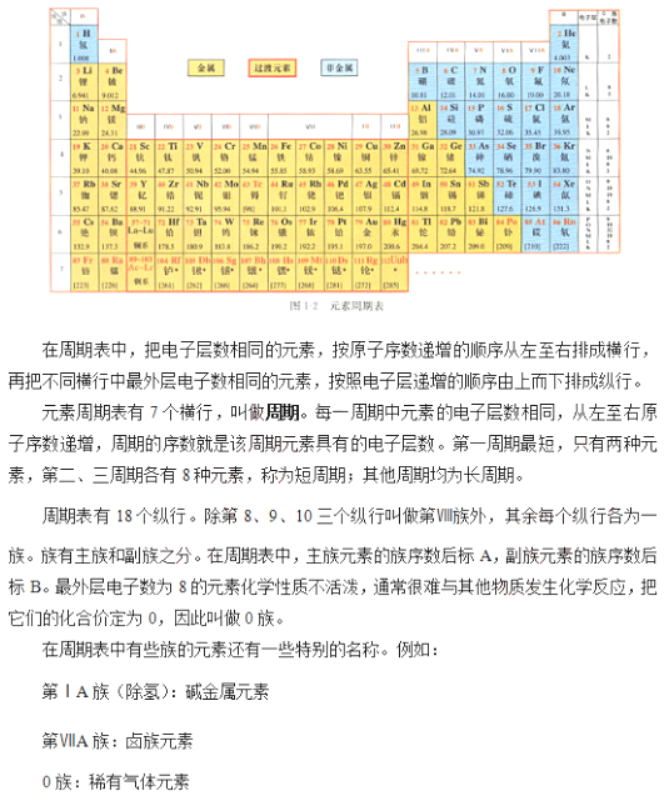
在周期表中,把电子层数相同的元素,按原子序数递增的顺序从左至右排成横行,再把不同横行中最外层电子数相同的元素,按照电子层递增的顺序由上而下排成纵行。
元素周期表有7个横行,叫做周期。每一周期中元素的电子层数相同,从左至右原子序数递增,周期的序数就是该周期元素具有的电子层数。第一周期最短,只有两种元素,第二、三周期各有8种元素,称为短周期;其他周期均为长周期。
周期表有18个纵行。除第8、9、10三个纵行叫做第Ⅷ族外,其余每个纵行各为一族。族有主族和副族之分。在周期表中,主族元素的族序数后标A,副族元素的族序数后标B。最外层电子数为8的元素化学性质不活泼,通常很难与其他物质发生化学反应,把它们的化合价定为0,因此叫做0族。
在周期表中有些族的元素还有一些特别的名称。例如:
第ⅠA族(除氢):碱金属元素
第ⅦA族:卤族元素
0族:稀有气体元素
3.基本要求:
(1)讲解直观,通俗易懂。
(2)重点讲解元素周期表的特点。
(3)板书工整有条理。
(4)要有提问环节
答辩题目1.简要概述元素周期表中元素的金属性和非金属性变化的规律
2.本节课的教学重难点是什么?
二、考题解析
【教学过程】
(一)故事导入
【讲故事】一天清晨,一位年轻人经过一个夜晚的研究后,疲倦地躺在书房的沙发上,他预感十五年来一直萦绕心头的问题即将迎刃而解,因此,这几个星期以来他格外地努力。十五年来,从他学生时代开始就一直对“元素”与“元素”之间可能存在的种种关联感兴趣,并且利用一切时间对化学元素进行研究。最近他感觉自己的研究大有进展,应该很快就能把元素间的关联和规律串在一起了。由于过度疲劳,他在不知不觉中睡着了。睡梦中,他突然清晰地看见元素排列成周期表浮现在他的眼前,他又惊又喜,随即清醒过来,顺手记下梦中的元素周期表。大家知道这个人是谁吗?
【学生回答】门捷列夫。
【教师引导】元素周期表的发现成了一项划时代的成就,而因为在梦中得到灵感,所以人们称为“天才的发现,实现在梦中。”但门捷列夫却不这么认为,把这个累积十五年的成就归功于“梦中的偶然”让他忿忿不平。他说:“在做那个梦以前,我一直盯着目标,不断努力、不断研究,梦中的景象只不过是我十五年努力的结果。”除了学习门捷列夫身上坚持不懈,投身科学的精神,今天我们也要认识他的这项伟大的成就——元素周期表。
(二)新课教学
【学生活动】五分钟时间翻开元素周期表,认识周期表及其中的元素。
【提出问题】周期表的结构是怎样的?周期表中一共有多少种元素?
【学生回答】有7横行,18纵列,总共包含了112种元素。
【教师总结】周期表中收录的是已经发现的元素,但是还有很多未知的元素等待人们去发现,所以周期表的科学性体现于它是在更新的。而在周期表中的横行叫做周期。
【提出问题】一共有几个周期?它们有什么区别?试着写出前3个周期的每个原子的结构示意图,并依次分析。
【学生回答,教师补充】元素周期表有7个周期。每一周期中元素的电子层数相同,从左至右原子序数递增,周期的序数就是该周期元素具有的电子层数。第一周期最短,只有两种元素,第二、三周期各有8种元素,称为短周期;其他周期均为长周期。
【教师提问】周期表中纵行的元素又有什么规律?按照上述同样的方法进行讨论交流。
【学生回答】周期表有18个纵行。除第8、9、10三个纵行叫做第Ⅷ族外,其余每个纵行各为一族。
【教师补充】18纵行总共分为16族,族有主族和副族之分。在周期表中,主族元素的族序数后标A,副族元素的族序数后标B。最外层电子数为8的元素化学性质不活泼,通常很难与其他物质发生化学反应,把它们的化合价定为0,因此叫做0族。
【教师提问】从周期表中,大家还可以发现哪些信息?
【学生回答】还可以看出每种原子的元素符号,相对原子质量。
【引导观察】周期表中哪些族有特殊的名称。
【学生回答】第ⅠA族(除氢):碱金属元素;第ⅦA族:卤族元素;0族:稀有气体元素
(三)拓展提高
【学生活动】画出前4周期的图,并填上原子。
(四)小结作业
小结:引导学生共同总结本节课的内容。
作业:思考同一周期或者同一主族的元素的化学性质有什么规律。
【板书设计】

1.简要概述元素周期表中元素的金属性和非金属性变化的规律。
2.本节课的教学重难点是什么?