下列分子和离子中,中心原子的价层电子对几何构型为四面体,且分子(离子)空间构型为角形(V形)的是()
第1题:
价层电子对互斥理论不适用于解释()。
第2题:
PCl3分子,中心原子采取()杂化,其几何构型为(),偶极矩()。
第3题:
A、3对
B、4对
C、5对
D、6对
第4题:
XeF4的中心原子的价层电子对数为()对,分子空间构型为()
第5题:
根据价层电子对互斥理论XeF2分子中,中心原子的电子构型为(),分子构型为()
第6题:
ABm型分子中,m=6,中心原子采取sp3d2杂化方式,则分子的空间几何构型是()。
第7题:
根据价层电子对互斥理论,下列分子或离子的空间构型是三角锥形的是()
第8题:


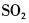
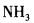
第9题:
根据价层电子对互斥理论,XeF4分子为正四面体结构
第10题:
对于AB型分子或离子的中心原子价层电子对数的确定1)中心原子价层电子对数=()2)若讨论的对象是离子(负或正)则中心原子的总电子数应()相应的离子电荷数