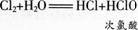(1)教学目标 【知识与技能目标】了解氯气与水反应的实质及产物;知道氯水的成分;认识次氯酸的性质和应用。
【过程与方法目标】通过观察、比较化学现象和反应,学会善于从实验中发现问题、分析问题、解决问题的方法。
【情感态度与价值观目标】通过实验激发学习化学的兴趣,树立将化学知识应用于生活、生产的意识。
(2)教学重、难点
【重点】氯气和水的反应、氯水的漂白性。
【难点】氯水的成分和漂白性。
(3)教学过程
环节一:导入新课
创设情景:有时候我们打开水龙头会闻到一股刺激性的气味,这种刺激性的气味来源于氯气,目前有很多自来水都采用氯气来杀菌、消毒,你知道这是为什么吗
导入:今天我们就来探索氯气和水的作用。
环节二:探究新知
对比启迪:我们知道二氧化碳能溶于水,与水反应生成碳酸,氯气能不能溶于水实验表明l体积的水大约溶解2体积的氯气.氯气的水溶液称之为氯水。氯气可以和水反应吗请同学们提出假设或猜想。
提问:如何证明氯气和水发生了反应请大家进行讨论。
【实验探究1】方案l:检验溶液的酸碱性,用玻璃棒蘸取少量的氯水点到紫色石蕊试纸上;方案2:检验氯离子,用胶头滴管吸取少量硝酸银置于小试管中,再用胶头滴管吸取少量氯水滴加到硝酸银溶液里。
请学生进行实验探究1并观察实验现象、得出结论。

设疑:在实验探究l中观察到湿润的蓝色石蕊试纸周围是红色的,它的中间部分是白色的,这意味着氯水中含有漂白性的物质。那氯水中具有漂白性的物质是什么首先我们要知道氯水中都存在哪些离子和分子。请大家根据已有知识进行讨论、推测。

这里我们考虑HCIO(次氯酸)和Cl---2到底是谁具有漂白性呢请学生思考讨论实验方案。
请学生进行实验探究并观察实验现象、得出结论。
【实验探究2】将氯气分别通入盛有干燥的红布条和湿润的红布条的广l:3瓶中,盖上玻璃片。
归纳:干燥的氯气无漂白性.潮湿的氯气有漂白性,所以可得具有漂白性的物质是HClO。

环节三:巩固练习
1.以下物质中,含有氯分子的是()。
A.液氯
B.氯水
C.盐酸
D.食盐
2.能使干燥有色布条褪色的物质是()。
A.氯气
B.氯化氢
C.氯水
D.液氯
环节四:小结作业
小结:这节课我们学习了哪些知识,请同学说一说。学生总结:氯气与水的反应原理,次氯酸的化学性质及应用。
作业:思考如何证明次氯酸的酸性比碳酸弱调研生活生产中还有哪些物质可以作为漂白剂,它们有什么区别
四、板书设计