0.05%
0.1%
0.2%
0.02%
第1题:
用氢氧化钠滴定液(0.1000mol/L)滴定20.00rnl盐酸溶液(0.1000mol/L),滴定突跃范围的pH值是
A.1.00~3.00
B.3.00~4.30
C.4.30~9.70
D.8.00~9.70
E.9.70~10.00
第2题:
用盐酸滴定液(0.1000mol/L)滴定20ml NH3·H20溶液(0.1000mol/L),化学计量点的pH值为( )。
A.9.94
B.9.70
C.8.72
D.7.O0
E.5.27
第3题:
用氢氧化钠滴定液(0.1000mol/L)滴定20ml醋酸溶液(0.1000mol/L),化学计量点的pH值为
A.8.72
B.7.O0
C.5.27
D.4.30
E.3.50
第4题:
用氢氧化钠滴定液(0.1000mol/L)滴定20.00ml盐酸溶液(0.1000mol/L),滴定突跃范围的pH是( )
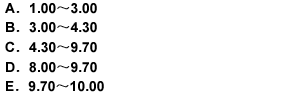
第5题:
A.pH>7.0
B.pH=7.0
C.pH<7.0
D.无法确定
第6题:
用氢氧化钠滴定液(0.1000mol/L)滴定20ml醋酸溶液(0.1000mol/L),化学计量点的pH值为( )。
A.8.72
B.7.OO
C.5.27
D.4.30
E.3.50
本题考查酸碱滴定法中化学计量点的计算。化学计量点时是醋酸钠溶液,溶液pH由Ac一的Kb和Cb决定,由于溶液体积增加一倍,Cb=0.5,[OH一]=(Kb×Cb)1/2一(Kw×Cb/Ka)1/2,经计算,pOH=5.28,pH=8.72。
第7题:
用氢氧化钠滴定液(0.1000mol/L)滴定20ml醋酸溶液(0.1000mol/L),化学计量点的pH为
A.8.72
B.7.00
C.5.27
D.4.3
E.3.5
第8题:
用盐酸滴定液(0.1000mol/L)滴定20mlNH4C1溶液(0.1000mol/L),化学计量点的pH值为
A.9.94
B.9.70
C.8.72
D.7.00
E.5.27
第9题:
A、3.00~4.00
B、3.00~4.30
C、4.30~9.70
D、8.00~9.70
E、9.70~10.00
第10题:
用0.1000mol/L NaOH溶液滴定20.00ml 0.1mol/L HAC溶液,滴定终点的PH值及选择指示剂为( )。
A.PH=8.7,酚酞
B.PH=7.0,甲基红
C.PH=9.7,酚酞
D.PH=6.2,甲基红